Строение альдегидов и кетонов

Альдегиды - органические вещества, молекулы которых содержат карбонильную группу :

соединенную с атомом водорода и углеводородным радикалом. Общая формула альдегидов имеет вид:

В простейшем альдегиде - роль углеводородного радикала играет другой атом водорода:
 Формальдегид
Формальдегид
Карбонильную группу, связанную с атомом водорода, часто называют альдегидной :

Кетоны - органические вещества, в молекулах которых карбонильная группа связана с двумя углеводородными радикалами. Очевидно, общая формула кетонов имеет вид:

Карбонильную группу кетонов называют кето-группой .
В простейшем кетоне - ацетоне - карбонильная группа связана с двумя метильными радикалами:

Номенклатура и изомерия альдегидов и кетонов
В зависимости от строения углеводородного радикала, связанного с альдегидной группой, различают предельные, непредельные, ароматические, гетероциклические и другие альдегиды :
В соответствии с номенклатурой ИЮПАК названия предельных альдегидов образуются от названия алкана с тем же числом атомов углерода с молекуле с помощью суффикса -аль . Например:
Нумерацию атомов углерода главной цепи начинают с атома углерода альдегидной группы. Поэтому альдегидная группа всегда располагается при первом атоме углерода, и указывать ее положение нет необходимости.
Наряду с систематической номенклатурой используют и тривиальные названия широко применяемых альдегидов. Эти названия, как правило, образованы от названий карбоновых кислот, соответствующих альдегидам.
Для названия кетонов по систематической номенклатуре кетогруппу обозначают суффиксом -он и цифрой, которая указывает номер атома углерода карбонильной группы (нумерацию следует начинать от ближайшего к кетогруппе конца цепи).
Например:
Для альдегидов характерен только один вид структурной изомерии - изомерия углеродного скелета , которая возможна с бутаналя, а для кетонов - также и изомерия положения карбонильной группы . Кроме этого, для них характерна и межклассовая изомерия (пропаналь и пропанон).
Физические свойства альдегидов и кетонов

В молекуле альдегида или кетона вследствие большей электроотрицательности атома кислорода по сравнению с углеродным атомом связь С=O сильно поляризована за счет смещения электронной плотности π-связи к кислороду:

Альдегиды и кетоны - полярные вещества с избыточной электронной плотностью на атоме кислорода . Низшие члены ряда альдегидов и кетонов (формальдегид, уксусный альдегид, ацетон) растворимы в воде неограниченно. Их температуры кипения ниже, чем у соответствующих спиртов. Это связано с тем, что в молекулах альдегидов и кетонов в отличие от спиртов нет подвижных атомов водорода и они не образуют ассоциатов за счет водородных связей.
Низшие альдегиды имеют резкий запах; у альдегидов, содержащих от четырех до шести атомов углерода в цепи, неприятный запах; высшие альдегиды и кетоны обладают цветочными запахами и применяются в парфюмерии.
Наличие альдегидной группы в молекуле определяет характерные свойства альдегидов.
Реакции восстановления.
1. Присоединение водорода к молекулам альдегидов происходит по двойной связи в карбонильной группе:

Продуктом гидрирования альдегидов являются первичные спирты, кетонов - вторичные спирты.
Так, при гидрировании уксусного альдегида на никелевом катализаторе образуется этиловый спирт, при гидрировании ацетона - пропанол-2.

2. Гидрирование альдегидов - реакция восстановления, при которой понижается степень окисления атома углерода, входящего в карбонильную группу.
Реакции окисления.
Альдегиды способны не только восстанавливаться, но и окисляться. При окислении альдегиды образуют карбоновые кислоты. Схематично этот процесс можно представить так:

1. Окисление кислородом воздуха. Например, из пропионового альдегида (пропаналя) образуется пропионовая кислота:

2. Окисление слабыми окислителями (аммиачный раствор оксида серебра). В упрощенном виде этот процесс можно выразить уравнением реакции:

Например:

Более точно этот процесс отражают уравнения:

Если поверхность сосуда, в котором проводится реакция, была предварительно обезжирена, то образующееся в ходе реакции серебро покрывает ее ровной тонкой пленкой. Поэтому эту реакцию называют реакцией «серебряного зеркала». Ее широко используют для изготовления зеркал, серебрения украшений и елочных игрушек.
3. Окисление свежеосажденным гидроксидом меди (II). Окисляя альдегид, Cu 2+ восстанавливается до Cu + . Образующийся в ходе реакции гидроксид меди (I) CuOH сразу разлагается на оксид меди (I) красного цвета и воду.

Эта реакция, так же как и реакция «серебряного зеркала », используется для обнаружения альдегидов.
Кетоны не окисляются ни кислородом воздуха, ни таким слабым окислителем, как аммиачный раствор оксида серебра.
Химические свойства альдегидов и кислот - конспект


Отдельные представители альдегидов и их значение
Формальдегид (метаналь, муравьиный альдегид HCHO) - бесцветный газ с резким запахом и температурой кипения -21 °С, хорошо растворим в воде. Формальдегид ядовит! Раствор формальдегида в воде (40 %) называют формалином и применяют для формальдегид и уксусной дезинфекции. В сельском хозяйстве формалин используют для протравливания семян, в кожевенной промышленности - для обработки кож. Формальдегид используют для получения уротропина - лекарственного вещества. Иногда спрессованный в виде брикетов уротропин применяют в качестве горючего (сухой спирт). Большое количество формальдегида расходуется при получении фенолформальдегидных смол и некоторых других веществ.
Уксусный альдегид (этаналь, ацетальдегид CH 3 CHO) - жидкость с резким, неприятным запахом и температурой кипения 21 °С, хорошо растворим в воде. Из уксусного альдегида в промышленных масштабах получают уксусную кислоту и ряд других веществ, он используется для производства различных пластмасс и ацетатного волокна. Уксусный альдегид ядовит !

Группа атомов -

Называется карбоксильной группой , или карбоксилом.
Органические кислоты, содержащие в молекуле одну карбоксильную группу, являются одноосновными .
Общая формула этих кислот RCOOH, например:

Карбоновые кислоты, содержащие две карбоксильные группы, называются двухосновными . К ним относятся, например, щавелевая и янтарная кислоты:

Существуют и многоосновные карбоновые кислоты, содержащие более двух карбоксильных групп. К ним относится, например, трехосновная лимонная кислота:

В зависимости от природы углеводородного радикала карбоновые кислоты делятся на предельные, непредельные, ароматические .
Предельными , или насыщенными, карбоновыми кислотами являются, например, пропановая (пропионовая) кислота:

или уже знакомая нам янтарная кислота.
Очевидно, что предельные карбоновые кислоты не содержат π-связей в углеводородном радикале.
В молекулах непредельных карбоновых кислот карбоксильная группа связана с ненасыщенным, непредельным углеводородным радикалом, например, в молекулах акриловой (пропеновой)
СН 2 =СН-СООН
или олеиновой
СН 3 -(СН 2) 7 -СН=СН-(СН 2) 7 -СООН
и других кислот.
Как видно из формулы бензойной кислоты, она является ароматической , так как содержит в молекуле ароматическое (бензольное) кольцо:


Название карбоновой кислоты образуется от названия соответствующего алкана (алкана с тем же числом атомов углерода в молекуле) с добавлением суффикса -ов — , окончания -ая и слова кислота . Нумерация атомов углерода начинается с карбоксильной группы . Например:

Количество карбоксильных групп указывается в названии префиксами ди-, три-, тетра- :
Многие кислоты имеют и исторически сложившиеся, или тривиальные, названия.
Состав предельных одноосновных карбоновых кислот будет выражаться общей формулой С n Н 2n O 2 , или С n Н 2n+1 СOOН , или RСООН .
Физические свойства карбоновых кислот
Низшие кислоты, т. е. кислоты с относительно небольшой молекулярной массой, содержащие в молекуле до четырех атомов углерода, - жидкости с характерным резким запахом (например, запах уксусной кислоты). Кислоты, содержащие от 4 до 9 атомов углерода, - вязкие маслянистые жидкости с неприятным запахом; содержащие более 9 атомов углерода в молекуле - твердые вещества, которые не растворяются в воде. Температуры кипения предельных одноосновных карбоновых кислот увеличиваются с ростом числа атомов углерода в молекуле и, следовательно, с ростом относительной молекулярной массы. Так, температура кипения муравьиной кислоты равна 100,8 °С, уксусной - 118 °С, пропионовой - 141 °С.
Простейшая карбоновая кислота - муравьиная НСООН, имея небольшую относительную молекулярную массу (М r (НСООН) = 46), при обычных уcловиях является жидкостью с температурой кипения 100,8 °С. В то же время бутан (M r (C 4 H 10) = 58) в тех же условиях газообразен и имеет температуру кипения -0,5 °С. Это несоответствие температур кипения и относительных молекулярных масс объясняется образованием димеров карбоновых кислот , в которых две молекулы кислоты связаны двумя водородными связями :

Возникновение водородных связей становится понятным при рассмотрении строения молекул карбоновых кислот.
Молекулы предельных одноосновных карбоновых кислот содержат полярную группу атомов - карбоксил

И практически неполярный углеводородный радикал . Карбоксильная группа притягивается молекулами воды, образуя с ними водородные связи:

Муравьиная и уксусная кислоты растворимы в воде неограниченно. Очевидно, что с увеличением числа атомов в углеводородном радикале растворимость карбоновых кислот снижается.
Химические свойства карбоновых кислот
Общие свойства, характерные для класса кислот (как органических, так и неорганических), обусловлены наличием в молекулах гидроксильной группы, содержащей сильную полярную связь между атомами водорода и кислорода. Рассмотрим эти свойства на примере растворимых в воде органических кислот.
1. Диссоциация с образованием катионов водорода и анионов кислотного остатка:
Более точно этот процесс описывает уравнение, учитывающее участие в нем молекул воды:
Равновесие диссоциации карбоновых кислот смещено влево; подавляющее большинство их - слабые электролиты. Тем не менее, кислый вкус, например, уксусной и муравьиной кислот объясняется диссоциацией на катионы водорода и анионы кислотных остатков.
Очевидно, что присутствием в молекулах карбоновых кислот «кислого» водорода, т. е. водорода карбоксильной группы, обусловлены и другие характерные свойства.
2. Взаимодействие с металлами , стоящими в электрохимическом ряду напряжений до водорода:
Так, железо восстанавливает водород из уксусной кислоты:
3. Взаимодействие с основными оксидами с образованием соли и воды:
4. Взаимодействие с гидроксидами металлов с образованием соли и воды (реакция нейтрализации):
5. Взаимодействие с солями более слабых кислот с образованием последних. Так, уксусная кислота вытесняет стеариновую из стеарата натрия и угольную из карбоната калия:

6. Взаимодействие карбоновых кислот со спиртами с образованием сложных эфиров - реакция этерификации (одна из наиболее важных реакций, характерных для карбоновых кислот):
Взаимодействие карбоновых кислот со спиртами катализируется катионами водорода.
Реакция этерификации обратима. Равновесие смещается в сторону образования сложного эфира в присутствии водоотнимающих средств и при удалении эфира из реакционной смеси.
В реакции, обратной этерификации, которая называется гидролизом сложного эфира (взаимодействие сложного эфира с водой), образуются кислота и спирт:

Очевидно, что реагировать с карбоновыми кислотами, т. е. вступать в реакцию этерификации, могут и многоатомные спирты, например, глицерин:

Все карбоновые кислоты (кроме муравьиной) наряду с карбоксильной группой содержат в молекулах углеводородный остаток. Безусловно, это не может не сказаться на свойствах кислот, которые определяются характером углеводородного остатка.
7. Реакции присоединения по кратной связи - в них вступают непредельные карбоновые кислоты. Например, реакция присоединения водорода - гидрирование. Для кислоты, содержащей в радикале одну л-связь, можно записать уравнение в общем виде:
Так, при гидрировании олеиновой кислоты образуется предельная стеариновая кислота:
Непредельные карбоновые кислоты, как и другие ненасыщенные соединения, присоединяют галогены по двойной связи. Так, например, акриловая кислота обесцвечивает бромную воду:

8. Реакции замещения (с галогенами) - в них способны вступать предельные карбоновые кислоты. Например, при взаимодействии уксусной кислоты с хлором могут быть получены различные хлорпроизводные кислоты:

Химические свойства карбоновый кислот - конспект



Отдельные представители карбоновых кислот и их значение
Муравьиная (метановая) кислота HCOOH - жидкость с резким запахом и температурой кипения 100,8 °C, хорошо растворима в воде.
Муравьиная кислота ядовита, при попадании на кожу вызывает ожоги! Жалящая жидкость, выделяемая муравьями, содержит эту кислоту.
Муравьиная кислота обладает дезинфицирующим свойством и поэтому находит свое применение в пищевой, кожевенной и фармацевтической промышленностях, медицине. Она используется при крашении тканей и бумаги.
Уксусная (этановая) кислота CH 3 COOH - бесцветная жидкость с характерным резким запахом, смешивается с водой в любых отношениях. Водные растворы уксусной кислоты поступают в продажу под названием уксуса (3-5 % -й раствор) и уксусной эссенции (70-80 %-й раствор) и широко используются в пищевой промышленности. Уксусная кислота - хороший растворитель многих органических веществ и поэтому используется при крашении, в кожевенном производстве, в лакокрасочной промышленности. Кроме этого, уксусная кислота является сырьем для получения многих важных в техническом отношении органических соединений: например, на ее основе получают вещества, используемые для борьбы с сорняками, - гербициды. Уксусная кислота является основным компонентом винного уксуса, характерный запах которого обусловлен именно ею. Она продукт окисления этанола и образуется из него при хранении вина на воздухе.
Важнейшими представителями высших предельных одноосновных кислот являются пальмитиновая C 15 H 31 COOH и стеариновая C 17 H 35 COOH кислоты . В отличие от низших кислот эти вещества твердые, плохо растворимы в воде.
Однако их соли - стеараты и пальмитаты - хорошо растворимы и обладают моющим действием, поэтому их еще называют мылами. Понятно, что эти вещества производят в больших масштабах.
Из непредельных высших карбоновых кислот наибольшее значение имеет олеиновая кислота C 17 H 33 COOH, или CH 3 - (CH 2) 7 - CH = CH -(CH 2) 7 COOH. Это маслоподобная жидкость без вкуса и запаха. Широкое применение в технике находят ее соли.
Простейшим представителем двухосновных карбоновых кислот является щавелевая (этандиовая) кислота HOOC-COOH, соли которой встречаются во многих растениях, например в щавеле и кислице. Щавелевая кислота - это бесцветное кристаллическое вещество, хорошо растворяется в воде. Она применяется при полировке металлов, в деревообрабатывающей и кожевенной промышленностях.
Справочный материал для прохождения тестирования:
Таблица Менделеева
Таблица растворимости
Альдегиды и кетоны имеют в своем составе карбонильную функциональную группу >С=О и относятся к классу карбонильных соединений. Также их называют оксосоединениями. Несмотря на то что эти вещества относятся к одному классу, из-за особенностей строения их все же разделяют на две большие группы.
В кетонах атом углерода из группы >С=О соединен с двумя одинаковыми или различными углеводородными радикалами, обычно они имеют вид: R-СО-R". Такую форму карбонильной группы называют еще кетогруппой или оксогруппой. В альдегидах же карбонильный углерод соединен только с одним углеводородным радикалом, а оставшаяся валентность занимается атомом водорода: R-СОН. Такую группу принято называть альдегидной. Благодаря этим различиям в строении альдегиды и кетоны ведут себя немного по-разному при взаимодействии с одними и теми же веществами.
Карбонильная группа
Атомы С и О в этой группе находятся в sp 2 -гибридизированном состоянии. Углерод за счет sp 2 -гибридных орбиталей имеет 3 σ-связи, расположенные под углом примерно в 120 градусов в одной плоскости.
Атом кислорода обладает гораздо большей электроотрицательностью, чем углеродный атом, а поэтому стягивает на себя подвижные электроны π-связи в группе >С=О. Поэтому на атоме О возникает избыточная электронная плотность δ - , а на атоме С, напротив, происходит ее уменьшение δ + . Этим и объясняются особенности свойств альдегидов и кетонов.
Двойная связь С=О более прочная, чем С=С, но вместе с тем и более реакционно способная, что объясняется большой разницей в электроотрицательностях атомов углерода и кислорода.
Номенклатура
Как и для всех других классов органических соединений, существуют различные подходы к наименованию альдегидов и кетонов. В соответствии с положениями номенклатуры ИЮПАК, наличие альдегидной формы карбонильной группы обозначается суффиксом -аль, а кетонной -он. Если карбонильная группа является старшей, то она определяет порядок нумерации атомов С в основной цепи. В альдегидной карбонильный атом углерода является первым, а в кетонах атомы С нумеруют с того края цепи, к которому ближе группа >С=О. С этим связана необходимость обозначать положение карбонильной группы в кетонах. Делают это, записывая соответствующую цифру после суффикса -он.
Если карбонильная группа не является старшей, то по правилам ИЮПАК ее наличие указывают приставкой -оксо для альдегидов и -оксо (-кето) для кетонов.
Для альдегидов широко применяют тривиальные названия, получаемые от наименования кислот, в которые они способны превращаться при окислении с заменой слова "кислота" на "альдегид":
- СΗ 3 -СОН уксусный альдегид;
- СΗ 3 -СН 2 -СОН пропионовый альдегид;
- СΗ 3 -СН 2 -СН 2 -СОН масляный альдегид.
Для кетонов распространены радикально функциональные названия, которые складываются из наименований левого и правого радикалов, соединенных с карбонильным атомом углерода, и слова "кетон":
- СΗ 3 -СО-СН 3 диметилкетон;
- СΗ 3 -СΗ 2 -СО-СН 2 -СН 2 -СН 3 этилпропилкетон;
- С 6 Η 5 -СО-СΗ 2 -СΗ 2 -СΗ 3 пропилфенилкетон.
Классификация
В зависимости от характера углеводородных радикалов класс альдегидов и кетонов делят на:
- предельные - атомы С связаны друг с другом только одинарными связями (пропаналь, пентанон);
- непредельные - между атомами С имеются двойные и тройные связи (пропеналь, пентен-1-он-3);
- ароматические - содержат в своей молекуле бензольное кольцо (бензальдегид, ацетофенон).
По числу карбонильных и наличию других функциональных групп различают:
- монокарбонильные соединения - содержат только одну карбонильную группу (гексаналь, пропанон);
- дикарбонильные соединения - содержат две карбонильные группы в альдегидной и/или кетонной форме (глиоксаль, диацетил);
- карбонильные соединения, содержащие также другие функциональные группы, которые, в свою очередь, делятся на галогенкарбонильные, гидроксикарбонильные, аминокарбонильные и т.д.
Изомерия
Наиболее характерной для альдегидов и кетонов является структурная изомерия. Пространственная возможна тогда, когда в углеводородном радикале присутствует асимметрический атом, а также двойная связь с различными заместителями.
- Изомерия углеродного скелета. Наблюдается у обоих типов рассматриваемых карбонильных соединений, но начинается с бутаналя в альдегидах и с пентанона-2 в кетонах. Так, бутаналь СН 3 -СΗ 2 -СΗ 2 -СОН имеет один изомер 2-метилпропаналь СΗ 3 -СΗ(СΗ 3)-СОН. А пентанон-2 СΗ 3 -СО-СΗ 2 -СΗ 2 -СΗ 3 изомерен 3-метилбутанону-2 СΗ 3 -СО-СΗ(СΗ 3)-СΗ 3 .
- Межклассовая изомерия. Оксосоединения с одинаковым составом изомерны между собой. Например, составу С 3Η 6 О соответствуют пропаналь СН 3 -СΗ 2 -СОН и пропанон СΗ 3 -СО-СΗ 3 . А молекулярная формула альдегидов и кетонов С 4 Н 8 О подходит бутаналю СН 3 -СΗ 2 -СΗ 2 -СОН и бутанону СН 3 -СО-СΗ 2 -СΗ 3 .
Также межклассовыми изомерами для карбоксильных соединений являются циклические оксиды. Например, этаналь и этиленоксид, пропанон и пропиленоксид. Кроме того, непредельные спирты и простые эфиры также могут иметь общий состав и оксосоединениями. Так, молекулярную формулу С 3 Н 6 О имеют:
- СΗ 3 -СΗ 2 -СОН - пропаналь;
- СΗ 2 =СΗ-СΗ 2 -ОН - ;
- СΗ 2 =СΗ-О-СН 3 - метилвиниловый эфир.
Физические свойства
Несмотря на то что молекулы карбонильных веществ полярны, в отличие от спиртов, альдегиды и кетоны не имеют подвижного водорода, а значит, не образуют ассоциатов. Следовательно, температуры плавления и кипения их несколько ниже, чем у соответствующих им спиртов.
Если сравнивать альдегиды и того же состава кетоны, то у последних t кип несколько выше. С увеличением молекулярной массы t пл и t кип оксосоединений закономерно повышаются.

Низшие карбонильные соединения (ацетон, формальдегид, уксусный альдегид) хорошо растворимы в воде, высшие же альдегиды и кетоны растворяются в органических веществах (спиртах, эфирах и т.д.).
Пахнут оксосоединения весьма различно. Низшие их представители имеют резкие запахи. Альдегиды, содержащие от трех до шести атомов С, пахнут очень неприятно, а вот высшие их гомологи наделены цветочными ароматами и даже применяются в парфюмерии.
Реакции присоединения
Химические свойства альдегидов и кетонов обусловлены особенностями строения карбонильной группы. Из-за того, что двойная связь С=О сильно поляризована, то под действием полярных агентов она легко переходит в простую одинарную связь.
1. Взаимодействие с синильной кислотой. Присоединение HCN в присутствии следов щелочей происходит с образованием циангидринов. Щелочь добавляют для повышения концентрации ионов CN - :
R-СОН + NCN ―> R-СН(ОН)-CN
2. Присоединение водорода. Карбонильные соединения легко могут восстанавливаться до спиртов, присоединяя водород по двойной связи. При этом из альдегидов получают первичные спирты, а из кетонов - вторичные. Реакции катализируются никелем:
Н 3 С-СОН + Н 2 ―> Н 3 С-СΗ 2 -ОΗ
Η 3 С-СО-СΗ 3 + Η 2 ―> Н 3 С-СΗ(ОΗ)-СΗ 3
3. Присоединение гидроксиламинов. Эти реакции альдегидов и кетонов катализируются кислотами:
Н 3 С-СОН + NH 2 OH ―> Η 3 С-СΗ=N-ОН + Н 2 О
4. Гидратация. Присоединение молекул воды к оксосоединениям приводит к образованию гем-диолов, т.е. таких двухатомных спиртов, в которых две гидроксильные группы присоединены к одному атому углерода. Однако такие реакции обратимы, полученные вещества тут же распадаются с образованием исходных веществ. Электроноакцепторные группы в данном случае смещают равновесие реакций в сторону продуктов:
>С=О + Η 2 <―> >С(ОΗ) 2
5. Присоединение спиртов. В ходе этой реакции могут получаться различные продукты. Если к альдегиду присоединяется две молекулы спирта, то образуется ацеталь, а если только одна, то полуацеталь. Условием проведения реакции является нагревание смеси с кислотой или водоотнимающим агентом.
R-СОН + НО-R" ―> R-СН(НО)-О-R"
R-СОН + 2НО-R" ―> R-СН(О-R") 2
Альдегиды с длинной углеводородной цепью склонны к внутримолекулярной конденсации, в результате которой образуются циклические ацетали.
Качественные реакции
Понятно, что при отличающейся карбонильной группе в альдегидах и кетонах химия их тоже различна. Порой необходимо понять, к какому из этих двух типов относится полученное оксосоединение. легче, чем кетоны, происходит это даже под действием оксида серебра или гидроксида меди (II). При этом карбонильная группа изменяется в карбоксильную и образуется карбоновая кислота.
Реакцией серебряного зеркала принято называть окисление альдегидов раствором оксида серебра в присутствии аммиака. Фактически в растворе образуется комплексное соединение, которое и воздействует на альдегидную группу:
Ag 2 O + 4NH 3 + Н 2 О ―> 2ОΗ
СΗ 3 -СОΗ + 2ОΗ ―> СН 3 -СОО-NH 4 + 2Ag + 3NH 3 +Н 2 О
Чаще записывают суть происходящей реакции более простой схемой:
СΗ 3 -СОΗ + Ag 2 O ―> СΗ 3 -СООΗ + 2Ag
В ходе реакции окислитель восстанавливается до металлического серебра и выпадает в осадок. При этом на стенках реакционного сосуда образуется тонкий серебряный налет, похожий на зеркало. Именно за это реакция и получила свое название.

Еще одной качественной реакцией, указывающей на разницу в строении альдегидов и кетонов, является действие на группу -СОН свежим Cu(OΗ) 2 . Готовят его добавлением щелочей к растворам солей меди двухвалентной. При этом образуется голубая суспензия, которая при нагревании с альдегидами меняет окраску на красно-коричневую за счет образования оксида меди (I):
R-СОН + Cu(OΗ) 2 ―> R-СООΗ + Cu 2 O + Η 2 О
Реакции окисления
Оксосоединения можно окислить раствором KMnO 4 при нагревании в кислой среде. Однако кетоны при этом разрушаются с образованием смеси продуктов, которые не имеют практической ценности.
Химическая реакция, отражающая данное свойство альдегидов и кетонов, сопровождается обесцвечиванием розоватой реакционной смеси. При этом из подавляющего большинства альдегидов получаются карбоновые кислоты:
СН 3 -СОН + KMnO 4 + H 2 SO 4 ―> СН 3 -СОН + MnSO 4 + K 2 SO 4 + Н 2 О
Формальдегид в ходе данной реакции окисляется до муравьиной кислоты, которая под действием окислителей распадается с образованием углекислого газа:
Н-СОН + KMnO 4 + H 2 SO 4 ―> СО 2 + MnSO 4 + K 2 SO 4 + Н 2 О
Для альдегидов и кетонов характерно полное окисление в ходе реакций горения. При этом образуются СО 2 и вода. Уравнение горения формальдегида имеет вид:
НСОН + O 2 ―> СО 2 + Н 2 О

Получение
В зависимости от объемов продуктов и целей их использования способы получения альдегидов и кетонов делят на промышленные и лабораторные. В химическом производстве карбонильные соединения получают окислением алканов и алкенов (нефтепродуктов), дегидрированием первичных спиртов и гидролизом дигалогеналканов.
1. Получение формальдегида из метана (при нагревании до 500 °С в присутствии катализатора):
СΗ 4 + О 2 ―> НСОН + Η 2 О.
2. Окисление алкенов (в присутствии катализатора и высокой температуре):
2СΗ 2 =СΗ 2 + О 2 ―> 2СН 3 -СОН
2R-СΗ=СΗ 2 + О 2 ―> 2R-СΗ 2 -СОΗ

3. Отщепление водорода от первичных спиртов (катализируется медью, необходимо нагревание):
СΗ 3 -СΗ 2 -ОН ―> СН 3 -СОН + Η 2
R-СН 2 -ОН ―> R-СОН + Н 2
4. Гидролиз дигалогеналканов щелочами. Обязательным условием является присоединенность обоих атомов галогенов к одному и тому же атому углерода:
СΗ 3 -C(Cl) 2 H + 2NaOH ―> СΗ 3 -СОΗ + 2NaCl + Н 2 О
В небольших количествах в лабораторных условиях карбонильные соединения получают гидратацией алкинов или окислением первичных спиртов.
5. Присоединение воды к ацетиленам происходит в присутствии в кислой среде (реакция Кучерова):
ΗС≡СΗ + Η 2 О ―> СН 3 -СОΗ
R-С≡СΗ + Η 2 О ―> R-СО-СН 3
6. Окисление спиртов с концевой гидроксильной группой проводят с использованием металлических меди или серебра, оксида меди (II), а также перманганатом или дихроматом калия в кислой среде:
R-СΗ 2 -ОΗ + О 2 ―> R-СОН + Н 2 О
Применение альдегидов и кетонов
Необходим для получения фенолформальдегидных смол, получаемых в ходе реакции его конденсации с фенолом. В свою очередь образующиеся полимеры необходимы для производства разнообразных пластмасс, древесно-стружечных плит, клея, лаков и многого другого. Также он применяется для получения лекарственных средств (уротропина), дезинфицирующих средств и используется для хранения биологических препаратов.

Основная часть этаналя идет на синтез уксусной кислоты и других органических соединений. Некоторые количества ацетальдегида используют в фармацевтическом производстве.
Ацетон широко применяется для растворения многих органических соединений, в числе которых лаки и краски, некоторых видов каучуков, пластмасс, природных смол и масел. Для этих целей он используется не только чистым, но и в смеси с другими органическими соединениями в составе растворителей марок Р-648, Р-647, Р-5, Р-4 и др. Также его используют для обезжиривания поверхностей при изготовлении различных деталей и механизмов. Большие количества ацетона требуются для фармацевтического и органического синтеза.
Многие альдегиды обладают приятными ароматами, благодаря чему применяются в парфюмерной промышленности. Так, цитраль имеет лимонный запах, бензальдегид пахнет горьким миндалем, фенилуксусный альдегид привносит в композицию аромат гиацинта.

Циклогексанон нужен для производства многих синтетических волокон. Из него получают адипиновую кислоту, в свою очередь применяемую как сырье для капролактама, нейлона и капрона. Также он используется в качестве растворителя жиров, природных смол, воска и ПВХ.
В молекулах этих соединений содержится двухвалентная карбонильная группа . В альдегидах она связана с одним атомом Н и с углеводородным радикалом, в кетонах - с двумя углеводородными радикалами:

Наличие и в альдегидах, и в кетонах карбонильной группы обусловливает определенное сходство их свойств. Однако имеются и различия, связанные с тем, что в молекулах альдегидов одна из связей карбонильной группы затрачивается на соединение с водородом; поэтому они содержат своеобразную альдегидную функциональную группу (или ). За счет водорода этой группы альдегиды очень легко окисляются, превращаясь в карбоновые кислоты (см. § 172). Так, при окислении уксусного альдегида образуется уксусная кислота, которую широко используют в промышленности и быту:

Вследствие легкой окисляемости альдегиды являются энергичными восстановителями; этим они существенно отличаются от кетонов, которые окисляются значительно труднее. Например, альдегиды восстанавливают оксид серебра (I) до металлического серебра (реакция серебряного зеркала - серебро осаждается на стенках сосуда, образуя зеркальный налет) и оксид Меди (II) до оксида :

Кетоны в этих условиях не окисляются, поэтому обе реакции используют как качественные, позволяющие отличить альдегиды от кетонов.
Альдегиды и кетоны можно получать окислением соответствующих спиртов, т. е. имеющих такой же углеродный скелет и гидроксильную группу при том же атоме углерода, который в получаемом альдегиде или кетоне образует карбонильную группу.
Например:

Муравьиный альдегид, или формальдегид, - газ с неприятным запахом, хорошо растворим в воде. Обладает антисептическими, а также дубящими свойствами. Водный раствор формальдегида (обычно ) называется формалином; он широко применяется для дезинфекции, консервирования анатомических препаратов, протравливания семян перед посевом и т. п. Значительные количества формальдегида используются для получения фенолоформальдегидных смол (см. § 177). Получают формальдегид из метилового спирта путем каталитического окисления его кислородом воздуха или путем дегидрирования (отщеплеиия водорода);
Эти реакции протекают при пропускании паров метилового спирта (в первом случае - в смеси с воздухом) над нагретыми катализаторами.
Уксусный альдегид, или ацетальдегид, . Легко кипящая бесцветная жидкость (темп. кип. 21 ), с характерным запахом прелых яблок, хорошо растворима в воде. В промышленности получается присоединением воды к ацетилену в присутствии солей в качестве катализатора;

Эта реакция, имеющая большое практическое значение, была открыта М. Г. Кучеровым (1850-1911). Уксусный альдегид затем может быть окислен в уксусную кислоту; его используют и для многих других синтезов.
Ацетон, или диметилкетон, . Бесцветная жидкость с характерным запахом (темп. кип. 56,2 ); смешивается с водой во всех соотношениях. Очень хороший растворитель многих органических веществ. Широко применяется в лакокрасочной промышленности, в производстве некоторых видов искусственного волокна, небьющегося органического стекла, кинопленки, бездымного пороха, для растворения ацетилена (в баллонах).
Ацетон используется также как исходное вещество для синтеза ряда органических соединений.
Первая группа свойств реакции присоединения. В карбонильной группе между углеродом и кислородом присутствует двойная связь, которая, как вы помните, состоит из сигма-связи и пи-связи. В реакциях присоединения пи-связь рвется и образуются две сигма связи одна с углеродом, вторая с кислородом. На углероде сосредоточен частичный положительный заряд, на кислороде частичный отрицательный. Поэтому к углероду присоединяется отрицательно заряженная частица реагента, анион, а к кислород положительно заряженная часть молекулы.
Первое свойство гидрирование, присоединение водорода.
Реакция проходит при нагревании. Применяется уже известный вам катализатор гидрирования никель. Из альдегидов получаются первичные спирты, из кетонов вторичные.
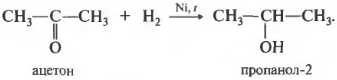
У вторичных спиртов гидроксогруппа связана со вторичным атомом углерода.
Второе свойство гидратация, присоединение воды. Эта реакция возможна только для формальдегида и ацетальдегида. Кетоны совсем не реагируют с водой.
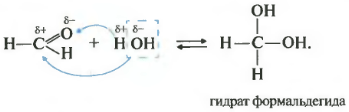
Все реакции присоединения идут таким образом, что плюс идет к минусу, а минус к плюсу.
Как вы помните из видео про спирты , наличие двух гидроксогрупп у одного атома почти невозможная ситуация, такие вещества крайне неустойчивы. Так вот конкретно два этих случая гидрат формальдегида и уксусного альдегида возможны, хотя и существуют только в растворе.
Сами реакции знать не обязательно. Скорее всего, вопрос на экзамене может звучать как констатация факта, допустим, с водой реагируют и перечислены вещества. Среди их перечня которых могут быть метаналь или этаналь.
Третье свойство присоединение синильной кислоты.

Снова плюс идет к минусу, а минус к плюсу. Получаются вещества, называемые гидроксинитрилами. Опять же, сама реакция встречается нечасто, но знать об этом свойстве нужно.
Четвертое свойство присоединение спиртов.
Здесь снова не нужно знать наизусть уравнение реакции, просто надо понимать, что такое взаимодействие возможно.

Как обычно в реакциях присоединения к карбонильной группе плюс к минусу, а минус к плюсу.
Пятое свойство реакция с гидросульфитом натрия.

И снова, реакция довольно сложная, выучить ее вряд ли получится, но это одна из качественных реакций на альдегиды, потому что полученная натриевая соль выпадает в осадок. То есть по факту вы должны знать, что альдегиды реагируют с гидросульфитом натрия, этого будет достаточно.
На этом закончим с первой группой реакций. Вторая группа реакции полимеризации и поликонденсации.
2. Полимеризация и поликонденсация альдегидов
С полимеризацией вы знакомы: полиэтилен, бутадиеновый и изопреновый каучуки, поливинилхлорид это продукты объединения множества молекул (мономеров) в одну большую, в единую полимерную цепь. То есть получается один продукт. При поликонденсации происходит то же самое, но помимо полимера получаются еще низкомолекулярные продукты, например, вода. То есть получается два продукта.
Итак, шестое свойство полимеризация. Кетоны в эти реакции не вступают, промышленное значение имеет только полимеризация формальдегида.
Пи-связь рвется и образуются две сигма связи с соседними мономерами. Получается полиформальдегид, называемый также параформ. Вероятнее всего, вопрос на экзамене может звучать так: в реакции полимеризации вступают вещества. И приведен список веществ, среди которых может быть в формальдегид.
Седьмое свойство поликонденсация. Еще раз: при поликонденсации помимо полимера получается еще низкомолекулярное соединение, например, вода. Формальдегид вступает в такую реакцию с фенолом. Для наглядности сначала запишем уравнение с двумя молекулами фенола.

В результате получается такой димер и отщепляется молекула воды. Теперь запишем уравнение реакции в общем виде.

Продуктом поликонденсации является феноло-формальдегидная смола. Она находит широкое применение от клеев и лаков до пластмасс и компонента древесно-стружечных плит.
Теперь третья группа свойств реакции окисления.
3. Окисление альдегидов и кетонов
Восьмой реакцией в общем списке является качественная реакция на альдегидную группу окисление аммиачным раствором оксида серебра. Реакция «серебряного зеркала». Скажу сразу, кетоны не вступают в эту реакцию, только альдегиды.

Альдегидная группа окисляется до карбоксильной, кислотной группы, но в присутствии аммиака, который является основание, сразу же происходит реакция нейтрализации и получается соль ацетат аммония. Серебро выпадает в осадок, покрывая пробирку изнутри и создавая зеркальную поверхность. Эта реакция встречается на ЕГЭ постоянно.
Кстати, эта же реакция является качественной на другие вещества, имеющие альдегидную группу, например, на муравьиную кислоту и ее соли, а также на глюкозу.
Девятая реакция тоже качественная на альдегидную группу окисление свежеосажденным гидроксидом меди два. Здесь тоже замечу, что кетоны не вступают в эту реакцию.

Визуально будет наблюдаться сначала образование желтого осадка, который потом становится красным. В некоторых учебниках встречается информация, что сначала образуется гидроксид меди один, имеющий желтый цвет, который затем распадается на красный оксид меди один и воду. Так вот это неверно по последним данным в процессе выпадения осадка меняется размер частиц оксида меди один, которые в конечном счете достигают размеров, окрашенных именно в красный цвет. Альдегид окисляется до соответствующей карбоновой кислоты. Реакция встречается на егэ очень часто.
Десятая реакция окисление альдегидов подкисленным раствором перманганата калия при нагревании.
Происходит обесцвечивание раствора. Альдегидная группа окисляется до карбоксильной, то есть альдегид окисляется до соответствующей кислоты. Для кетонов эта реакция не имеет практического смысла, поскольку происходит разрушение молекулы и в результате получается смесь продуктов.
Важно отметить, что муравьиный альдегид, формальдегид, окисляется до углекислого газа, потому как соответствующая ему муравьиная кислота сама не устойчива к действию сильных окислителей.
В итоге углерод переходит из степени окисления 0 в степень окисления +4. Напомню, что и метанол, как правило, в таких условиях окисляется по максимуму до CO 2 , проскакивая стадию и альдегида, и кислоты. Эту особенность надо запомнить.
Одиннадцатая реакция горение, полное окисление. И альдегиды, и кетоны сгорают до углекислого газа и воды.
Запишем уравнение реакции в общем виде.
По закону сохранения массы атомов слева должно быть столько же, сколько атомов справа. Потому что ведь в химических реакциях атомы никуда не деваются, а просто изменяется порядок связей между ними. Так вот молекул углекислого газа будет столько же, сколько и атомов углерода в молекуле карбонильного соединения, поскольку в состав молекулы входит один атом углерода. То есть n молекул CO 2 . Молекул воды будет в два раза меньше, чем атомов водорода, то есть 2n/2, а значит просто n.
Атомов кислорода слева и справа одинаковое количество. Справа их 2n из углекислого газа, потому что в каждой молекуле два атома кислорода, плюс n воды, итого 3n. Слева атомов кислорода столько же 3n, но один из атомов находится в молекуле альдегида, значит его надо вычесть из общего количества, чтобы получить количество атомов, приходящихся на молекулярный кислород. Выходит 3n-1 атомов содержит молекулярный кислород, а значит молекул в 2 раза меньше, потому как в состав одной молекулы входят 2 атома. То есть (3n-1)/2 молекул кислорода.
Таким образом, мы составили уравнение сгорания карбонильных соединений в общем виде.
И, наконец, двенадцатое свойство, относящееся к реакциям замещения галогенирование по альфа-атому углерода. Еще раз обратимся к строению молекулы альдегида. Кислород оттягивает на себя электронную плотность, создавая частичный положительный заряд а углероде. Метильная группа пытается компенсировать этот положительный заряд, смещая к нему электроны от водорода по цепи сигма-связей. Связь углерод-водород становится более полярной и водород легче отрывается при атаке реагентом. Такой эффект наблюдается только для альфа-атома углерода, то есть атома следующего за альдегидной группой, вне зависимости от длины углеводородного радикала.
Таким образом, возможно получение, например, 2-хлорацетальдегида. Возможно дальнейшее замещение атомов водорода до трихлорэтаналя.
Слово альдегид было придумано как сокращение латинского alcohol dehydrogenatus - дегидрированный спирт, самый популярный альдегид - формальдегид, из него делают смолы, синтезируют лекарства и как консервант. Формула альдегида - R-CHO, соединение, в котором карбонильная группа соединена с водородом и радикалом.
Слово кетон произошло от слова ацетон, младшего соединения из семейства кетонов. Кетоны используются как растворители, лекарства и для синтеза полимеров. Формула кетона - R-C(O)-R, соединение, в котором карбонильная группа соединена с двумя радикалами.
Структура и свойства карбонильной группы
Карбонильная группа основана на связи атома углерода и атома кислорода посредством α- и π-связей. Резонансная структура группы определяет высокую полярность соединения и электронное облако сдвинуто в сторону кислорода: C δ+ =O δ- . Введение электроотрицательных элементов в уменьшает полярность связи, повышая положительный заряд молекулы. Нуклеофильные заместители увеличивают отрицательный заряд кислорода.
Атом углерода в карбонильной группе является сильным электрофилом (присоединяет электроны), поэтому большинство реакций альдегидов и кетонов осуществляется нуклеофильными реактивами (основания Льюиса). Логично, атом кислорода является сильным нуклеофилом, и реакции с атомом кислорода возможны с применением электрофилов (кислот Льюиса).
Реакция карбонильной группы с основанием Льюиса
(R)(R)C δ+ =O δ- + B: → (R)(R)C(B)-O
Реакция карбонильной группы с кислотой Льюиса
(R)(R)C δ+ =O δ- + Y: → (R)(R)C-O-Y
В дополнение, неразделённые электроны кислорода наделяют его слабыми свойствами основания, поэтому те альдегиды и цетоны, которые не растворяются в воде, растворяются в концентрированной серной кислоте.
Физические свойства карбонильной группы
Высокая полярность связи C=O образует высокий дипольный момент, из-за чего носители карбоксильной группы имеют более высокую температуру кипения, по сравнению с углеводородами.
Неразделённые электроны в атоме кислорода образуют водородную связь с молекулами воды, поэтому, начиная с пяти атомов углерода в радикалах, альдегиды и кетоны плохо растворяются в воде или не растворяются вовсе.
Альдегиды и кетоны, имеющие до 12 атомов углерода - жидкости. Алифатические соединения с карбонильной группой имеют плотность примерно 0.8, поэтому плавают на поверхности воды, циклогексанон имеет плотность около единицы, ароматические альдегиды и кетоны имеют плотность чуть больше, чем плотность воды.
Реакции альдегидов и кетонов
Присоединение воды
В процессе реакции воды с альдегидами и кетонами образуются диолы (гликоли, двухатомные спирты). Реакция протекает с использованием катализатора - кислотой или основанием и является двусторонней:
RR-CO + H-OH ↔ R R\ C /OH -OH
Присоединение нуклеофильных углеродов
Важные нуклеофильные соединения, реагирующие с альдегидами и кетонами - металлорганические соеденинения (органические соединения, в молекулах которых существует связь атома металла с атомом/атомами углерода). Одни из представителей металлорганических соединений - реактивы Гриньяра (общая формула - R-Mg-X), в реакциях с альдегидами и кетонами образуют спирты:
RH-C=O + R-C - H 2 -Mg + -Cl - → RH-С-(O-MgCl)(CH 2 -R)
RH-С-(O-MgCl)(CH 2 -R) + H-OH → RH-C-CH 2 R + OH-Mg-Cl
Окисление альдегидов и кетонов
При окислении, альдегиды находятся на промежуточном этапе между спиртами и карбоновыми кислотами:
В присутствии водорода и кислорода:
R-CH 2 -OH ↔ R-C(=O)-H ↔ R-COOH
Альдегиды легко окисляются, что позволяет использовать более мягкие окислители, чем простой кислород. Ароматические альдегиды подвергаются окислению легче, чем алифатические. Проблема окисления альдегидов - в образовании побочных продуктов.
Кетоны окисляются с трудом, для окисления кетонов необходимо использовать сильные окислители и большое количество тепла. В результате окисления разрывается связь C-C и образовывается кислота (есть исключение):
В присутствии KMnO 4 , H и большого количества тепла :
CH 3 -C(=O)-CH 2 CH 3 → CH 3 -C(=O)-OH + CH 3 CH 2 -C(=O)-OH
Исключением является окисление диоксидом селена, SeO 2 , метил-группа, следующая за карбонильной, окисляется, преобразовываясь в другую карбонильную группу. Например, метилэтилкетон окисляется в диацетил:
Окисление метилэтилкетона в диацетил:
CH 3 CH 2 -C(=O)-CH 3 + SeO 2 → CH 3 -C(=O)-C(=O)-CH 3 + H 2 O + Se
Лёгкость, с которой окисляются альдегиды, позволяет легко отличить их от кетонов, для этого используются мягкие окислители, такие как: реактив Толленса (гидроксид диамминсеребра, Ag(NH 3) 2 OH), реактив Фелинга (алкалиновый раствор ионов меди Cu в Сегнетовой соли KNaC 4 H 6 O 6 ·4H 2 O) и раствор Бенедикта (ионы меди с цитратом и карбонатом натрия). Ароматические альдегиды реагируют с реактивом Толленса, но не реагируют с реактивами Бенедикта и Фелинга, что используется для определения количества алифатических и ароматных альдегидов.
Полимеризация альдегидов
Паральдегид
Ацетальдегид имеет температуру кипения 20°C, что затрудняет его хранение и применение. При обработке ацетальдегида кислотой при низкой температуре, ацетальдегид соединяется в цикличную тройную молекулу - паральдегид, с температурой кипения 120°C. Паральдегид при небольшом нагреве деполимеризуется, высвобождая три молекулы ацетальдегида.
Формальдегид
Для удобства транспортировки и хранения, формальдегид продаётся не в форме газа, а в виде формалина - водного раствора с содержанием 37-40% параформальдегида, OH(CH 2 O) n H, со средним значением n=30. Параформальдегид - белое аморфное вещество, твёрдое, получаемое медленным выпариванием формалина при низком давлении. Полимеризация происходит за счёт присоединения друг к другу молекул формальдегида:
CH 2 =O + H 2 O ↔
+ n → HO-(CH 2 O) n+1 -H
Полимер Дерлин (полиоксиметилен) является хорошим линейным пластиком с высокой молекулярной массой, дерлин обладает отличными характеристиками прочности и эластичности.

